編者按:近來,有部分專家稱疫情第二波感染高峰或於3-5月到來。對於第二輪疫情是否到來、何時到來也一直是公眾關注的焦點。想要應對新冠病毒感染大流行,還必須要確保新冠病毒疫苗的有效性及公平分配。但新冠病毒的快速變異、疫苗的供應短缺、公眾對疫苗的不信任、“疫苗民族主義”等不利因素正在影響全球新冠病毒免疫工作的正常進行。本文作者就全球新冠病毒疫苗的研發及接種概況進行了闡述和總結,供讀者參考。
導讀 · 2023.02.07
近來,有部分專家稱疫情第二波感染高峰或於3-5月到來。對於第二輪疫情是否到來、何時到來也一直是公眾關注的焦點。自新冠病毒疫情大流行以來,全世界一直在積極研發新冠病毒疫苗。其中一些國家在短短的一年內就成功研發出多款新冠病毒疫苗——鑑於一款新疫苗的研發週期通常為8至15年,這樣的情況是前所未有的。
想要應對新冠病毒感染大流行,還必須要確保新冠病毒疫苗的有效性及公平分配。但新冠病毒的快速變異、疫苗的供應短缺、公眾對疫苗的不信任、“疫苗民族主義”等不利因素正在影響全球新冠病毒免疫工作的正常進行。本文作者就全球新冠病毒疫苗的研發及接種概況進行了闡述和總結,供讀者參考。
全球新冠病毒疫苗的接種概況
目前,全球共有30多種不同類型的新冠病毒疫苗獲得了國際社會的認可。截至2022年底,全球接種了130多億劑疫苗。從接種人口比例來看,許多國家約四分之三的人口已完成了全程疫苗接種,其中卡塔爾、新加坡和阿聯酋是全球新冠病毒疫苗接種率最高的國家,如圖1所示。雖然全球新冠病毒疫苗接種率正在上升,但全球仍有近三分之一的人口尚未接種疫苗,例如,非洲地區的新冠病毒疫苗接種率為全球最低。
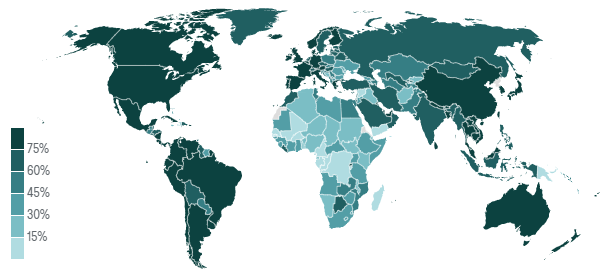
圖1:全球新冠病毒疫苗接種率
(截至2022年12月4日)
一些國家為了提高新冠病毒疫苗接種率,採取了強制接種疫苗措施。意大利和沙特要求公務員和企業員工必須接種新冠病毒疫苗。美國也曾計劃採取相關措施,但最終被最高法院否決。中國提倡全民接種新冠病毒疫苗,但未做強制要求。有些國家僅出台了針對醫護人員的強制接種疫苗的規定。總之,全球疫苗接種工作仍困難重重,尤其是老年人的疫苗接種工作。此外,兒童將獲得更多接種新冠病毒疫苗的機會。在中國,3歲及以上的兒童可接種疫苗;在美國,6個月及以上的兒童符合接種疫苗的資格。
新冠病毒疫苗的設計原理
全球上市的新冠病毒疫苗主要分為兩種類型:一是中國研發的“滅活疫苗”;二是西方國家研發的“信使核糖核酸(mRNA)疫苗”。 “滅活疫苗”的設計原理是利用抗原觸發免疫系統中的防禦性白細胞,產生能夠與病毒結合和中和的抗體;而“信使核糖核酸疫苗”的設計原理是利用喪失活性或活性減弱的病毒或從病毒中分離出的蛋白質來引起免疫反應。美國輝瑞(Pfizer)公司、德國生物新技術(BioNTech)公司以及美國莫德納(Moderna)公司研發的新冠病毒疫苗均屬於“信使核糖核酸(mRNA)疫苗”。
與“信使核糖核酸(mRNA)疫苗”不同,美國諾瓦瓦克斯醫藥(Novavax)公司研發的新冠病毒疫苗屬於“重組蛋白疫苗”。該疫苗利用新冠病毒表面的刺突蛋白來引起免疫反應。此外,一些新冠病毒疫苗利用病毒載體或不同病毒的改良版本來引起免疫反應,屬於“腺病毒疫苗”,例如英國—瑞典合資的阿斯利康製藥(AstraZeneca)公司研發的新冠病毒疫苗。
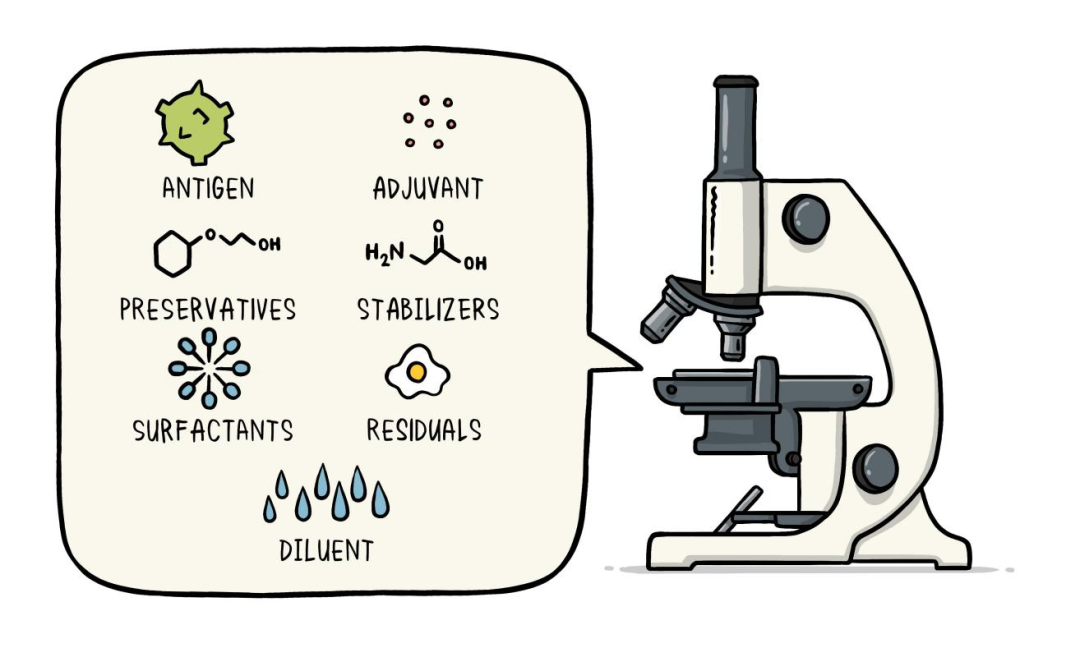
疫苗是如何開發的?
(圖源:WHO)
當社區的大部分人(群體)對某種病原體產生免疫力時,即形成了群體免疫。當實現群體免疫時,病原體便不太可能在人與人之間傳播。人類對水痘、麻疹、腮腺炎和小兒麻痺症的群體免疫均是通過接種疫苗實現的。然而,有專家認為,鑑於全球新冠病毒疫苗接種率的不均衡、公眾對新冠病毒疫苗的不信任以及新冠病毒的變異,人類仍無法實現對新冠病毒的群體免疫。
新冠病毒疫苗研發的主要參與者
新冠病毒疫苗的研發離不開社會各界的參與和支持,其中一些疫苗是製藥公司與政府機構、研究機構合作的結晶。以下為新冠病毒疫苗研發的主要參與者:
(一)政府機構
政府機構在新冠病毒疫苗研發中發揮著關鍵作用。例如,美國於2020年啟動了一項名為“曲速行動”(Operation Warp Speed)的新冠病毒疫苗研發計劃。該計劃採取政府和社會資本合作的方式進行,目的是加快新冠病毒疫苗的研發,並確保為3億美國人提供足夠的疫苗劑量。 “曲速行動”的規模龐大,有多個政府機構共同參與,包括美國疾病控制與預防中心(CDC)、美國國立衛生研究院(NIH)、美國食品藥品管理局(FDA)、美國生物醫學高級研究與發展局(BARDA)、美國國防部等。 “曲速行動”計劃的最終預算為180億美元,參與該計劃的製藥公司將得到數十億美元的資助。歐盟於2020年舉辦了“應對新冠肺炎疫情國際認捐大會”,籌集了74億歐元用於新冠病毒疫苗的研發。
(二)多邊機構
世界衛生組織、世界銀行等多邊機構致力於支持全球新冠病毒疫苗的融資和生產,以及確保疫苗的公平分配。 2020年,流行病防範創新聯盟(由惠康信託基金會和比爾與美琳達·蓋茨基金會共同成立,旨在通過加速疫苗研發防控流行性疾病的國際聯盟)與全球疫苗免疫聯盟(旨在幫助中低收入國家獲取疫苗的全球衛生合作組織)、世界衛生組織共同提出並牽頭啟動“新冠病毒疫苗實施計劃”,擬於2021年底前向全球提供20億劑新冠病毒疫苗。截至2022年11月,該計劃已向全球提供了約18億劑疫苗。

輝瑞向COVAX(新冠肺炎疫苗實施計劃)提供疫苗(圖源:輝瑞)
(三)製藥公司
製藥公司極大地推動了全球新冠病毒疫苗的研發進程。無論是中小型還是大型製藥公司,均專注於新冠病毒疫苗的研發。製藥公司的疫苗初期研發通常會獲得公共資助(例如美國國立衛生研究院的資助),相當於政府為製藥公司承擔了部分風險。但臨床研發的大部分資金仍由製藥公司承擔。
(四)研究機構和非營利組織
許多高校參與了新冠病毒疫苗的臨床研發。例如,2020年,牛津大學詹納研究所與阿斯利康製藥公司宣布合作研發新冠病毒疫苗。此外,蓋茨基金會一直是資助新冠病毒疫苗研發的主要非營利組織之一。
新冠病毒疫苗的研發進展
全球絕大多數獲世界衛生組織批准的新冠病毒疫苗均由美國、中國和俄羅斯研發。數據顯示,西方國家研發的“信使核糖核酸(mRNA)疫苗”在預防新冠病毒感染方面具有顯著優勢,是目前全球最受歡迎的新冠病毒疫苗之一。中國研發的“滅活疫苗”已向全球分發了數十億劑。俄羅斯研發的“類毒素疫苗”是全球誕生的首個新冠病毒疫苗。
除已上市的疫苗外,仍有幾十款新冠病毒疫苗處於大規模臨床試驗階段,200多種新冠病毒疫苗處於初期臨床試驗階段。美國流行病學家奧斯特霍爾姆(Michael Osterholm)表示,未來肯定會有新冠病毒疫苗2.0、3.0乃至4.0版本,但目前仍難以確保疫苗應對病毒變異的有效性。
新冠病毒疫苗的研發過程
新冠病毒疫苗的研發十分複雜,可分為6個階段:理論研究(2至4年);初期臨床試驗(2年);臨床試驗(5年);藥物註冊(1年);藥物生產(2年);藥物分發(3至6個月)。
臨床試驗的目的是評估疫苗的關鍵指標。與其他疫苗一樣,新冠病毒疫苗在臨床試驗前,必須在動物活體上試驗。在臨床試驗階段,科研人員會根據疫苗的試驗結果逐步增加疫苗試驗者的數量。如果疫苗未引起免疫反應、產生有害的副作用或與上市疫苗過於相似,科研人員便會終止相關研究。臨床試驗通常是以“盲法”進行的,即一部分疫苗試驗者接種疫苗,另一部分接種安慰劑。

疫苗研發
(圖源:WTO)
如果疫苗成功通過了臨床試驗,製藥公司便可向國家或國際藥品監管機構申請藥品註冊。在美國,僅不到10%的藥物能夠成功通過臨床試驗。在獲得上市批准前,製藥公司可向美國食品藥品管理局申請“緊急使用授權”(允許銷售未經批准的醫療用品)。此外,疫苗還必須獲得其他國家的藥品監管機構的使用許可,才能在國際市場銷售。待疫苗獲得使用許可後,便可批量生產。 2021年8月,美國輝瑞公司和德國生物新技術公司的疫苗獲得了美國食品藥品管理局的使用許可,隨後美國莫德納公司的疫苗於2022年1月也獲得了美國食品藥品管理局的使用許可。
雖然世界衛生組織不負責藥物審批,但製藥公司可要求世界衛生組織對藥物進行資格預審,以確保藥物符合國際標準,許多中低收入國家對此十分重視。世界衛生組織的緊急使用清單是為了應對突發公共衛生事件,將未獲得使用許可的醫療用品納入採購範圍的技術審評程序,目前已有11種新冠病毒疫苗列入了該清單。
全球加速研發新冠病毒疫苗
在正常情況下,研發一款新疫苗的完整週期為8至15年。在新冠病毒大流行之前,最短的疫苗研發週期為4年。在新冠病毒大流行之後,全球科研人員通過多個疫苗研發階段並行及新興疫苗技術的支持,大幅縮短了疫苗的研發週期。數據顯示,新冠病毒疫苗的研發週期為12至18個月。

WHO、WIPO、WTO舉行
聯合技術研討會呼籲創新與合作
(圖源:WHO)
最典型的例子是美國的“曲速行動”計劃。為了加速新冠病毒疫苗的生產及交付,該計劃允許製藥公司在臨床試驗階段批量生產候選疫苗;在美國莫德納公司的疫苗獲得美國食品藥品管理局的使用許可之前,美國政府通過“曲速行動”計劃”向其支付了25億美元,用於購買1億劑新冠病毒疫苗。美國政府與美國輝瑞公司和德國生物新技術公司簽訂了19.5億美元的合同,計劃購買上述兩家公司合作研發的新冠病毒疫苗;拜登就職美國總統後,美國向中低收入國家捐贈了超過10億劑疫苗。
縮短疫苗研發週期的另一種方法是研發新的疫苗技術。 “信使核糖核酸(mRNA)疫苗”和“重組蛋白疫苗”的研發週期較短,而傳統疫苗則需要幾個月的時間在動物或昆蟲細胞中培養抗原。
新冠病毒感染的非疫苗療法
除接種疫苗外,目前已有幾十種針對新冠病毒感染的療法。雖然非疫苗療法無法用於預防新冠病毒感染,但可減輕患者病情的嚴重程度及縮短病情的持續時間。研究表明,美國吉利德科學(Gilead Sciences)公司研發的一種新型實驗性廣譜抗病毒藥物瑞德西韋(Remdesivir) 的療效顯著,接受該藥物治療的新冠病毒重症患者的死亡率較低。此外,也有研究指出,地塞米松(一種常見的類固醇)可降低新冠病毒重症患者的死亡率。美國食品藥品監督管理局已批准新冠病毒康復者恢復期血漿的緊急使用。雖然恢復期血漿療法已廣泛用於治療許多其他疾病,但仍存在一定的風險。因此,捐獻的血液必須進行安全性檢測。一些患者可能會出現輕微的並發症或完全沒有並發症。其他一些患者可能會出現嚴重甚至致命的並發症。
此外,一些製藥公司已成功研發出治療新冠病毒肺炎的口服藥,例如輝瑞和默克(Merck Drugs & Biotechnology)分別研發的帕克斯洛維德(Paxlovid)和莫納皮拉韋(Molnupiravir)。美國退伍軍人事務部(VA)的一項研究發現,在感染或症狀消失後服用帕克洛維德,可減輕新冠病毒患者的後遺症。
新冠病毒疫苗面臨的挑戰
儘管多款新冠病毒疫苗已上市,各國不斷加大新冠病毒疫苗的生產力度以及多邊機構也一直積極協調新冠病毒疫苗的分配,但目前全球新冠病毒疫苗的生產和分配能力仍遠遠低於所需水平。
在疫苗供應十分有限的情況下,各國不得不為爭奪疫苗而展開博弈。早在新冠病毒疫情大流行初期,澳大利亞、加拿大、美國等高收入國家就與全球製藥公司簽訂了新冠病毒疫苗的採購協議,此舉導致了發展中國家難以獲得足夠的疫苗供應,只有中國和印度是例外,其龐大的製藥產業使其能夠確保自身的疫苗供應。外交關係委員會資深研究員博利基(Thomas J. Bollyky)警告稱,“疫苗民族主義”會長期導致疫苗分配的不平等,進而導致疫情的反彈。
但從積極的一面來看,國際社會一直致力於解決全球新冠病毒疫苗短缺的問題。在2021年“全球新冠病毒峰會”上,美國表示支持世界衛生組織到明年9月為全世界至少70%的人口接種疫苗的目標。此外,世界貿易組織成員國在第12屆部長會議中達成協議,允許發展中國家在未獲得新冠病毒疫苗專利持有方授權的情況下,在本國生產和出口新冠病毒疫苗,以增加發展中國家的疫苗供應。由於跨國製藥公司拒絕分享新冠病毒疫苗知識產權,一些中低收入國家在世界衛生組織的支持下也開始研發“信使核糖核酸(mRNA)疫苗”。

WHO發布全球COVID-19疫苗接種戰略更新
以覆蓋未受保護人群
(圖源:WHO)
與此同時,新冠病毒的變種“奧密克戎”及其亞變種的蔓延,引起了全球對現有新冠病毒疫苗有效性的擔憂。有鑑於此,許多國家鼓勵符合疫苗接種條件的人群,盡快完成疫苗加強針的接種。但世界衛生組織強調,應優先為未接種疫苗的人群完成疫苗接種。
除上述挑戰外,公眾對短時間內研發出的新冠病毒疫苗缺乏信心。 2021年一項關於公眾對新冠病毒疫苗接受度的調查顯示,在23個國家中,約有四分之一的公眾對新冠病毒疫苗持懷疑態度。美國公共衛生協會(APHA)執行主任本傑明(Georges C. Benjamin)稱,美國政府目前仍無法向公眾交代接種和不接種疫苗的差別,也無法說服對疫苗持懷疑態度者接種疫苗。
本文作者
克萊爾·克洛布西斯塔(Claire Klobucista):美國外交關係委員會(Council on Foreign Relations)副主編。
*免責聲明:本文所闡述觀點僅代表作者本人立場,不代表大灣區評論或IIA機構立場。
*本文內容原載於IPP評論,譯者曾輝。
GBA Review 新傳媒
評論文章
 如何“破局”与“共融”?——百川论坛“变革中的‘全球南方’:地缘政治与发展合作”2025研讨会在深启幕
如何“破局”与“共融”?——百川论坛“变革中的‘全球南方’:地缘政治与发展合作”2025研讨会在深启幕 練卓文:加強中歐合作應對當前的國際貿易挑戰
練卓文:加強中歐合作應對當前的國際貿易挑戰 包宏:美元——特朗普發動全球關稅戰的根源、底氣與死穴|經濟觀察
包宏:美元——特朗普發動全球關稅戰的根源、底氣與死穴|經濟觀察 王希聖:從「重新武裝歐洲計畫」到《歐洲防務白皮書》 ,歐洲安全能否離開美國?|戰略與安全
王希聖:從「重新武裝歐洲計畫」到《歐洲防務白皮書》 ,歐洲安全能否離開美國?|戰略與安全 俠客島對話鄭永年:我們要「超越關稅看關稅」
俠客島對話鄭永年:我們要「超越關稅看關稅」 俠客島對話鄭永年:特朗普關稅「休克療法」能醫治「美國病」嗎
俠客島對話鄭永年:特朗普關稅「休克療法」能醫治「美國病」嗎 鄭永年、段嘯林、袁冉東:深圳下一步發展的「三個共識」|全球灣區觀察
鄭永年、段嘯林、袁冉東:深圳下一步發展的「三個共識」|全球灣區觀察 中國和美國拼的是「經濟韌性」|獨思錄 x 鄭永年
中國和美國拼的是「經濟韌性」|獨思錄 x 鄭永年 「中美俄大三角」關係的現狀及其未來|獨思錄 x 鄭永年
「中美俄大三角」關係的現狀及其未來|獨思錄 x 鄭永年 遊傳滿:如何「鉗制」DeepSeek?OpenAI如是說|全球法治觀察
遊傳滿:如何「鉗制」DeepSeek?OpenAI如是說|全球法治觀察