导读 · 2023.02.07
近来,有部分专家称疫情第二波感染高峰或于3-5月到来。对于第二轮疫情是否到来、何时到来也一直是公众关注的焦点。自新冠病毒疫情大流行以来,全世界一直在积极研发新冠病毒疫苗。其中一些国家在短短的一年内就成功研发出多款新冠病毒疫苗——鉴于一款新疫苗的研发周期通常为8至15年,这样的情况是前所未有的。
想要应对新冠病毒感染大流行,还必须要确保新冠病毒疫苗的有效性及公平分配。但新冠病毒的快速变异、疫苗的供应短缺、公众对疫苗的不信任、“疫苗民族主义”等不利因素正在影响全球新冠病毒免疫工作的正常进行。本文作者就全球新冠病毒疫苗的研发及接种概况进行了阐述和总结,供读者参考。
全球新冠病毒疫苗的接种概况
目前,全球共有30多种不同类型的新冠病毒疫苗获得了国际社会的认可。截至2022年底,全球接种了130多亿剂疫苗。从接种人口比例来看,许多国家约四分之三的人口已完成了全程疫苗接种,其中卡塔尔、新加坡和阿联酋是全球新冠病毒疫苗接种率最高的国家,如图1所示。虽然全球新冠病毒疫苗接种率正在上升,但全球仍有近三分之一的人口尚未接种疫苗,例如,非洲地区的新冠病毒疫苗接种率为全球最低。
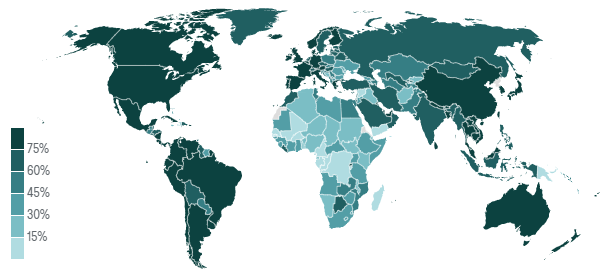
图1:全球新冠病毒疫苗接种率
(截至2022年12月4日)
一些国家为了提高新冠病毒疫苗接种率,采取了强制接种疫苗措施。意大利和沙特要求公务员和企业员工必须接种新冠病毒疫苗。美国也曾计划采取相关措施,但最终被最高法院否决。中国提倡全民接种新冠病毒疫苗,但未做强制要求。有些国家仅出台了针对医护人员的强制接种疫苗的规定。总之,全球疫苗接种工作仍困难重重,尤其是老年人的疫苗接种工作。此外,儿童将获得更多接种新冠病毒疫苗的机会。在中国,3岁及以上的儿童可接种疫苗;在美国,6个月及以上的儿童符合接种疫苗的资格。
新冠病毒疫苗的设计原理
全球上市的新冠病毒疫苗主要分为两种类型:一是中国研发的“灭活疫苗”;二是西方国家研发的“信使核糖核酸(mRNA)疫苗”。“灭活疫苗”的设计原理是利用抗原触发免疫系统中的防御性白细胞,产生能够与病毒结合和中和的抗体;而“信使核糖核酸疫苗”的设计原理是利用丧失活性或活性减弱的病毒或从病毒中分离出的蛋白质来引起免疫反应。美国辉瑞(Pfizer)公司、德国生物新技术(BioNTech)公司以及美国莫德纳(Moderna)公司研发的新冠病毒疫苗均属于“信使核糖核酸(mRNA)疫苗”。
与“信使核糖核酸(mRNA)疫苗”不同,美国诺瓦瓦克斯医药(Novavax)公司研发的新冠病毒疫苗属于“重组蛋白疫苗”。该疫苗利用新冠病毒表面的刺突蛋白来引起免疫反应。此外,一些新冠病毒疫苗利用病毒载体或不同病毒的改良版本来引起免疫反应,属于“腺病毒疫苗”,例如英国—瑞典合资的阿斯利康制药(AstraZeneca)公司研发的新冠病毒疫苗。
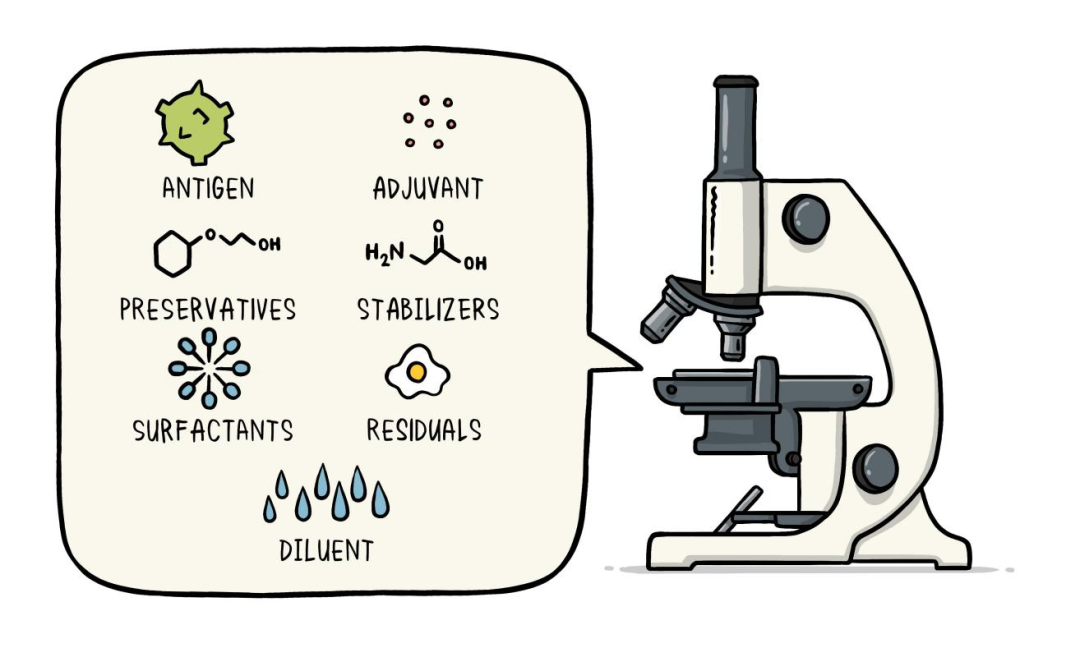
疫苗是如何开发的?
(图源:WHO)
当社区的大部分人(群体)对某种病原体产生免疫力时,即形成了群体免疫。当实现群体免疫时,病原体便不太可能在人与人之间传播。人类对水痘、麻疹、腮腺炎和小儿麻痹症的群体免疫均是通过接种疫苗实现的。然而,有专家认为,鉴于全球新冠病毒疫苗接种率的不均衡、公众对新冠病毒疫苗的不信任以及新冠病毒的变异,人类仍无法实现对新冠病毒的群体免疫。
新冠病毒疫苗研发的主要参与者
新冠病毒疫苗的研发离不开社会各界的参与和支持,其中一些疫苗是制药公司与政府机构、研究机构合作的结晶。以下为新冠病毒疫苗研发的主要参与者:
(一)政府机构
政府机构在新冠病毒疫苗研发中发挥着关键作用。例如,美国于2020年启动了一项名为“曲速行动”(Operation Warp Speed)的新冠病毒疫苗研发计划。该计划采取政府和社会资本合作的方式进行,目的是加快新冠病毒疫苗的研发,并确保为3亿美国人提供足够的疫苗剂量。“曲速行动”的规模庞大,有多个政府机构共同参与,包括美国疾病控制与预防中心(CDC)、美国国立卫生研究院(NIH)、美国食品药品管理局(FDA)、美国生物医学高级研究与发展局(BARDA)、美国国防部等。“曲速行动”计划的最终预算为180亿美元,参与该计划的制药公司将得到数十亿美元的资助。欧盟于2020年举办了“应对新冠肺炎疫情国际认捐大会”,筹集了74亿欧元用于新冠病毒疫苗的研发。
(二)多边机构
世界卫生组织、世界银行等多边机构致力于支持全球新冠病毒疫苗的融资和生产,以及确保疫苗的公平分配。2020年,流行病防范创新联盟(由惠康信托基金会和比尔与美琳达·盖茨基金会共同成立,旨在通过加速疫苗研发防控流行性疾病的国际联盟)与全球疫苗免疫联盟(旨在帮助中低收入国家获取疫苗的全球卫生合作组织)、世界卫生组织共同提出并牵头启动“新冠病毒疫苗实施计划”,拟于2021年底前向全球提供20亿剂新冠病毒疫苗。截至2022年11月,该计划已向全球提供了约18亿剂疫苗。

辉瑞向COVAX(新冠肺炎疫苗实施计划)提供疫苗(图源:辉瑞)
(三)制药公司
制药公司极大地推动了全球新冠病毒疫苗的研发进程。无论是中小型还是大型制药公司,均专注于新冠病毒疫苗的研发。制药公司的疫苗初期研发通常会获得公共资助(例如美国国立卫生研究院的资助),相当于政府为制药公司承担了部分风险。但临床研发的大部分资金仍由制药公司承担。
(四)研究机构和非营利组织
许多高校参与了新冠病毒疫苗的临床研发。例如,2020年,牛津大学詹纳研究所与阿斯利康制药公司宣布合作研发新冠病毒疫苗。此外,盖茨基金会一直是资助新冠病毒疫苗研发的主要非营利组织之一。
新冠病毒疫苗的研发进展
全球绝大多数获世界卫生组织批准的新冠病毒疫苗均由美国、中国和俄罗斯研发。数据显示,西方国家研发的“信使核糖核酸(mRNA)疫苗”在预防新冠病毒感染方面具有显著优势,是目前全球最受欢迎的新冠病毒疫苗之一。中国研发的“灭活疫苗”已向全球分发了数十亿剂。俄罗斯研发的“类毒素疫苗”是全球诞生的首个新冠病毒疫苗。
除已上市的疫苗外,仍有几十款新冠病毒疫苗处于大规模临床试验阶段,200多种新冠病毒疫苗处于初期临床试验阶段。美国流行病学家奥斯特霍尔姆(Michael Osterholm)表示,未来肯定会有新冠病毒疫苗2.0、3.0乃至4.0版本,但目前仍难以确保疫苗应对病毒变异的有效性。
新冠病毒疫苗的研发过程
新冠病毒疫苗的研发十分复杂,可分为6个阶段:理论研究(2至4年);初期临床试验(2年);临床试验(5年);药物注册(1年);药物生产(2年);药物分发(3至6个月)。
临床试验的目的是评估疫苗的关键指标。与其他疫苗一样,新冠病毒疫苗在临床试验前,必须在动物活体上试验。在临床试验阶段,科研人员会根据疫苗的试验结果逐步增加疫苗试验者的数量。如果疫苗未引起免疫反应、产生有害的副作用或与上市疫苗过于相似,科研人员便会终止相关研究。临床试验通常是以“盲法”进行的,即一部分疫苗试验者接种疫苗,另一部分接种安慰剂。

疫苗研发
(图源:WTO)
如果疫苗成功通过了临床试验,制药公司便可向国家或国际药品监管机构申请药品注册。在美国,仅不到10%的药物能够成功通过临床试验。在获得上市批准前,制药公司可向美国食品药品管理局申请“紧急使用授权”(允许销售未经批准的医疗用品)。此外,疫苗还必须获得其他国家的药品监管机构的使用许可,才能在国际市场销售。待疫苗获得使用许可后,便可批量生产。2021年8月,美国辉瑞公司和德国生物新技术公司的疫苗获得了美国食品药品管理局的使用许可,随后美国莫德纳公司的疫苗于2022年1月也获得了美国食品药品管理局的使用许可。
虽然世界卫生组织不负责药物审批,但制药公司可要求世界卫生组织对药物进行资格预审,以确保药物符合国际标准,许多中低收入国家对此十分重视。世界卫生组织的紧急使用清单是为了应对突发公共卫生事件,将未获得使用许可的医疗用品纳入采购范围的技术审评程序,目前已有11种新冠病毒疫苗列入了该清单。
全球加速研发新冠病毒疫苗
在正常情况下,研发一款新疫苗的完整周期为8至15年。在新冠病毒大流行之前,最短的疫苗研发周期为4年。在新冠病毒大流行之后,全球科研人员通过多个疫苗研发阶段并行及新兴疫苗技术的支持,大幅缩短了疫苗的研发周期。数据显示,新冠病毒疫苗的研发周期为12至18个月。

WHO、WIPO、WTO举行
联合技术研讨会呼吁创新与合作
(图源:WHO)
最典型的例子是美国的“曲速行动”计划。为了加速新冠病毒疫苗的生产及交付,该计划允许制药公司在临床试验阶段批量生产候选疫苗;在美国莫德纳公司的疫苗获得美国食品药品管理局的使用许可之前,美国政府通过“曲速行动”计划”向其支付了25亿美元,用于购买1亿剂新冠病毒疫苗。美国政府与美国辉瑞公司和德国生物新技术公司签订了19.5亿美元的合同,计划购买上述两家公司合作研发的新冠病毒疫苗;拜登就职美国总统后,美国向中低收入国家捐赠了超过10亿剂疫苗。
缩短疫苗研发周期的另一种方法是研发新的疫苗技术。“信使核糖核酸(mRNA)疫苗”和“重组蛋白疫苗”的研发周期较短,而传统疫苗则需要几个月的时间在动物或昆虫细胞中培养抗原。
新冠病毒感染的非疫苗疗法
除接种疫苗外,目前已有几十种针对新冠病毒感染的疗法。虽然非疫苗疗法无法用于预防新冠病毒感染,但可减轻患者病情的严重程度及缩短病情的持续时间。研究表明,美国吉利德科学(Gilead Sciences)公司研发的一种新型实验性广谱抗病毒药物瑞德西韦(Remdesivir) 的疗效显著,接受该药物治疗的新冠病毒重症患者的死亡率较低。此外,也有研究指出,地塞米松(一种常见的类固醇)可降低新冠病毒重症患者的死亡率。美国食品药品监督管理局已批准新冠病毒康复者恢复期血浆的紧急使用。虽然恢复期血浆疗法已广泛用于治疗许多其他疾病,但仍存在一定的风险。因此,捐献的血液必须进行安全性检测。一些患者可能会出现轻微的并发症或完全没有并发症。其他一些患者可能会出现严重甚至致命的并发症。
此外,一些制药公司已成功研发出治疗新冠病毒肺炎的口服药,例如辉瑞和默克(Merck Drugs & Biotechnology)分别研发的帕克斯洛维德(Paxlovid)和莫纳皮拉韦(Molnupiravir)。美国退伍军人事务部(VA)的一项研究发现,在感染或症状消失后服用帕克洛维德,可减轻新冠病毒患者的后遗症。
新冠病毒疫苗面临的挑战
尽管多款新冠病毒疫苗已上市,各国不断加大新冠病毒疫苗的生产力度以及多边机构也一直积极协调新冠病毒疫苗的分配,但目前全球新冠病毒疫苗的生产和分配能力仍远远低于所需水平。
在疫苗供应十分有限的情况下,各国不得不为争夺疫苗而展开博弈。早在新冠病毒疫情大流行初期,澳大利亚、加拿大、美国等高收入国家就与全球制药公司签订了新冠病毒疫苗的采购协议,此举导致了发展中国家难以获得足够的疫苗供应,只有中国和印度是例外,其庞大的制药产业使其能够确保自身的疫苗供应。外交关系委员会资深研究员博利基(Thomas J. Bollyky)警告称,“疫苗民族主义”会长期导致疫苗分配的不平等,进而导致疫情的反弹。
但从积极的一面来看,国际社会一直致力于解决全球新冠病毒疫苗短缺的问题。在2021年“全球新冠病毒峰会”上,美国表示支持世界卫生组织到明年9月为全世界至少70%的人口接种疫苗的目标。此外,世界贸易组织成员国在第12届部长会议中达成协议,允许发展中国家在未获得新冠病毒疫苗专利持有方授权的情况下,在本国生产和出口新冠病毒疫苗,以增加发展中国家的疫苗供应。由于跨国制药公司拒绝分享新冠病毒疫苗知识产权,一些中低收入国家在世界卫生组织的支持下也开始研发“信使核糖核酸(mRNA)疫苗”。

WHO发布全球COVID-19疫苗接种战略更新
以覆盖未受保护人群
(图源:WHO)
与此同时,新冠病毒的变种“奥密克戎”及其亚变种的蔓延,引起了全球对现有新冠病毒疫苗有效性的担忧。有鉴于此,许多国家鼓励符合疫苗接种条件的人群,尽快完成疫苗加强针的接种。但世界卫生组织强调,应优先为未接种疫苗的人群完成疫苗接种。
除上述挑战外,公众对短时间内研发出的新冠病毒疫苗缺乏信心。2021年一项关于公众对新冠病毒疫苗接受度的调查显示,在23个国家中,约有四分之一的公众对新冠病毒疫苗持怀疑态度。美国公共卫生协会(APHA)执行主任本杰明(Georges C. Benjamin)称,美国政府目前仍无法向公众交代接种和不接种疫苗的差别,也无法说服对疫苗持怀疑态度者接种疫苗。
本文作者
克莱尔·克洛布西斯塔(Claire Klobucista):美国外交关系委员会(Council on Foreign Relations)副主编。
*免责声明:本文所阐述观点仅代表作者本人立场,不代表大湾区评论或IIA机构立场。
*本文内容原载于IPP评论,译者曾辉。
GBA Review 新传媒

